
Le modificazioni quantitative e qualitative età-correlate del tessuto muscolare e il declino della forza muscolare costituiscono due aspetti fondamentali di una tipica sindrome geriatrica definita sarcopenia. La sarcopenia è attualmente codificata nel sistema internazionale di classificazione delle patologie (International Classification Disease, ICD-10), all’interno della macrocategoria “patologie del sistema muscoloscheletrico e del tessuto connettivo” (codice ICD-10: M62.84). La rilevanza di tale condizione non è da attribuirsi solo all’elevata prevalenza, legata all’invecchiamento globale della popolazione, ma anche alle sue importanti implicazioni su disabilità, qualità di vita e mortalità.
Le premesse
L’invecchiamento è caratterizzato da una riduzione del peso corporeo, che inizia intorno alla sesta decade di vita e diviene più marcata dopo i 75 anni. Pur perdendo peso, le persone tendono ad accumulare massa grassa, fino ai 75 anni; dopo tale età, la massa grassa inizia a diminuire, accelerando così la perdita di peso corporeo. In questa trasformazione si assiste inoltre a un fenomeno di ridistribuzione del tessuto adiposo in alcune sedi principali, quali addome, fegato, muscolatura scheletrica, tessuto cardiaco e midollo osseo. Parallelamente, già dalla quarta decade di vita la massa muscolare inizia a subire un declino, che diviene più marcato con il progredire dell’età.
Queste modifiche quantitative possono associarsi a modifiche qualitative e funzionali, che includono una riduzione della forza muscolare e della performance fisica. La velocità e l’ampiezza di questi cambiamenti sono influenzate da diversi fattori fisiologici, parafisiologici e patologici: sesso, etnia, livello di attività fisica, stato nutrizionale e metabolico, patologie croniche (es. diabete), funzioni cognitive, allettamento e immobilizzazione.
Si stima che la prevalenza globale di sarcopenia, definita secondo i criteri indicati nel 2018 dall’EWGSOP European Working Group on Sarcopenia in Older People, sia dell’11% (Cruz-Jentoft, et al., 2019). In termini di differenze etnia-specifiche, tale condizione sembra più frequente nella popolazione non-asiatica rispetto a quella asiatica. Tuttavia, quando si parla di sarcopenia si deve tenere conto dell’altissima variabilità nella popolazione dovuta alla definizione usata, al metodo di misurazione di massa e forza muscolare e performance fisica. Indipendentemente dalla definizione utilizzata si può comunque osservare un rapporto stretto tra prevalenza di sarcopenia ed età: questa condizione si manifesta più frequentemente con l’aumentare dell’età, soprattutto dopo i 65 anni.
Nella prevalenza di sarcopenia un aspetto estremamente interessante rispetto alle differenze di genere è che queste sembrano manifestarsi in modo più o meno marcato in base al contesto sanitario che viene considerato; ad esempio, all’interno del setting ospedaliero si ritrovano valori sostanzialmente eguali tra uomini e donne, mentre nelle case di riposo e nelle strutture di lungodegenza si osserva un incremento del 20% circa di prevalenza di sarcopenia negli uomini rispetto alle donne.
Sarcopenia: una definizione in continua evoluzione
Le definizioni proposte sono numerose e ancora oggi manca una definizione unica e universalmente accettata, che risulti applicabile in tutte le popolazioni e in tutti i gruppi etnici. Il termine sarcopenia fu introdotto da Irwin Rosenberg nel 1988, per descrivere la riduzione età-correlata della massa muscolare. Nella sua connotazione originale, il concetto di sarcopenia prevedeva come principale elemento la riduzione in quantità della muscolatura scheletrica; la riduzione di forza, invece, rappresentava un epifenomeno conseguente alla perdita di massa muscolare (Rosenberg, 1997).
Negli ultimi trent’anni, le nuove evidenze scientifiche hanno sottolineato come la riduzione della forza muscolare sia più marcata e solo parzialmente giustificata dalla riduzione della massa muscolare. Questo ha portato a una modifica del paradigma di sarcopenia, con l’introduzione di nuove definizioni che hanno dato maggior risalto alle modificazioni della forza muscolare.
Nel 2008 è stato introdotto il concetto di dynapenia per descrivere la riduzione isolata della forza muscolare (Clark, Manini, 2008). L’introduzione degli aspetti funzionali, degli effetti della riduzione di massa e della forza muscolare sulla performance fisica ha determinato un’ulteriore evoluzione nel paradigma della sarcopenia. È il 2010 quando l’EWGSOP pubblica la sua prima definizione di sarcopenia come sindrome geriatrica caratterizzata da una perdita progressiva e generalizzata della massa e della forza muscolare scheletrica associata a un aumentato rischio di eventi avversi, quali disabilità, scarsa qualità di vita e infine morte. Sul piano operativo, la sarcopenia veniva descritta come caratterizzata dalla compresenza di una ridotta massa muscolare e di una ridotta funzionalità muscolare (intesa come forza muscolare o performance). La sola riduzione della massa muscolare definiva la condizione di pre-sarcopenia, mentre la compromissione di tutti e tre i parametri (massa, forza, performance) caratterizzava lo stadio di sarcopenia severa (Cruz-Jentoft, et al., 2010).
Dopo qualche anno, l’EWGSOP pubblica una versione aggiornata della definizione e delle linee guida sulla sarcopenia (EWGSOP2). Se le linee guida del 2010 ponevano sullo stesso piano la riduzione della massa e della forza, che dovevano essere entrambe presenti per poter diagnosticare una condizione di sarcopenia, le linee guida del 2018 mettono al centro la riduzione della forza, che diviene il principale fattore per la definizione operativa della sarcopenia. La dimostrazione della riduzione della quantità o della qualità del muscolo scheletrico viene utilizzata per confermare la diagnosi, mentre la scarsa performance fisica viene impiegata come indice di severità della condizione (Cruz-Jentoft, et al., 2019).
Negli anni in cui il gruppo di ricerca europeo pubblicava il suo primo consensus per la definizione e la diagnosi di sarcopenia, un gruppo di ricerca statunitense, il Foundation for the National Institutes of Health (FNIH) Sarcopenia Project, lavorava per produrre proprie linee guida. Il FNIH Sarcopenia Project nasceva sotto il patrocinio del FNIH Biomarkers Consortium, con lo scopo di individuare, mediante un approccio evidence-based, i parametri clinici e rispettivi cut-off da impiegare nella diagnosi di sarcopenia. Era noto da tempo, infatti, che una ridotta massa muscolare si associava a debolezza, a sua volta fortemente legata a limitazione funzionale e disabilità. Tali evidenze indussero FNIH Sarcopenia Project a includere sia la riduzione di massa che il declino della forza nella definizione di sarcopenia, come condizione caratterizzata da limitazione funzionale in presenza di debolezza (riduzione della forza o dynapenia), conseguente alla riduzione della massa muscolare (Studenski, et al., 2014).
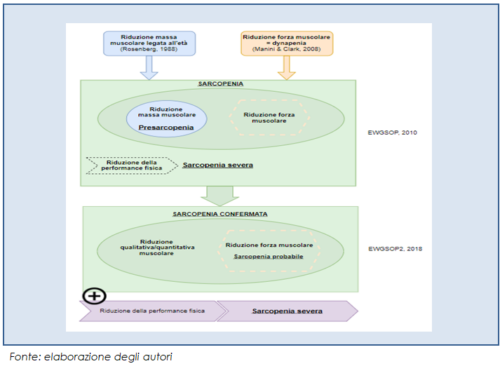
(secondo criteri EWGSOP 2010 e EWGSOP2 2018)
Utilizzando la definizione dell’EWGSOP2 si possono individuare diversi stadi di sarcopenia e si può tracciare un continuum di progressione patologica della sindrome. Partendo dalla condizione in cui l’individuo presenta normale forza muscolare, la comparsa di una riduzione di tale forza definisce la sarcopenia probabile. La ridotta forza muscolare abbinata alla riduzione qualitativa e quantitativa della massa muscolare definisce la sarcopenia confermata. Infine, quando a questi elementi si associa anche una ridotta performance fisica si delinea la sarcopenia severa. Non è ancora ben chiaro se e con quanta probabilità sia possibile la regressione da uno stato di sarcopenia più severo a uno stato meno severo.
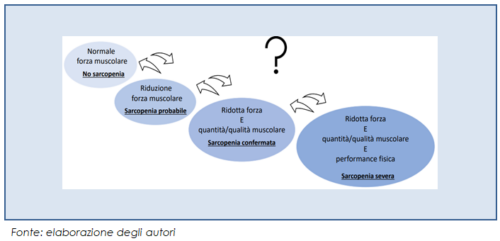
Per chiarire questo particolare aspetto, recenti studi su popolazioni di anziani hanno evidenziato come nel tempo siano possibili transizioni sia peggiorative che migliorative tra gli stadi di sarcopenia (Trevisan, et al., 2022). In particolare, lo stato della sarcopenia probabile (stadio intermedio tra assenza di sarcopenia e sarcopenia confermata) sembra essere il più dinamico, anche rispetto alla probabilità di regredire verso l’assenza di sarcopenia. L’entità e i fattori associati a questa possibile regressione sono di estrema importanza e attualità: ulteriori approfondimenti in questo ambito sono cruciali, al fine di ottimizzare la pianificazione di interventi preventivi rivolti alla popolazione anziana.
Sarcopenia: eziopatogenesi e fattori di rischio
Il muscolo scheletrico è costituito da fibrocellule muscolari (miociti), tessuto connettivo di sostegno e tessuto adiposo. Con il processo di invecchiamento si assiste a una progressiva riduzione dei motoneuroni α, “centrali” e unità motorie fondamentali ad alta velocità di conduzione, deputate a innervare le fibre muscolari scheletriche. Questa riduzione di unità motorie e quindi del numero di fibre muscolari avviene principalmente per fenomeni di apoptosi e neurotossicità cellulare, promosse da stress ossidativo e infiammazione cronica. Nel processo di sviluppo della sarcopenia si assiste anche a una variazione nella tipologia di fibre muscolari; in particolar modo si osserva una conversione maggiore delle fibre muscolari di tipo II (a contrazione rapida) a fibre muscolari di tipo I (a contrazione lenta).
I meccanismi biologici coinvolti nella patogenesi della sarcopenia sono molteplici: per questo si parla di genesi multifattoriale, soprattutto nel soggetto anziano. Nello specifico, la sarcopenia è il risultato di uno squilibrio tra i processi anabolici e catabolici a livello muscolare. Si è osservato che la sarcopenia viene favorita da condizioni in cui da un lato si riduce l’anabolismo muscolare, cioè la costruzione e la rigenerazione del tessuto, dall’altro aumenta il catabolismo muscolare, ovvero la distruzione e degenerazione delle fibre muscolari. Di conseguenza, tutti i fattori che agiscono aumentando il catabolismo e/o riducendo l’anabolismo del muscolo possono essere considerati fattori di rischio per la sarcopenia.
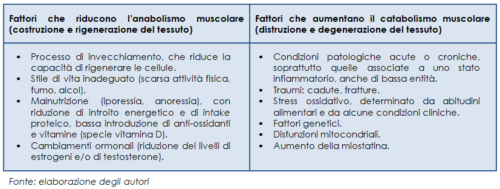
Riguardo alle condizioni patologiche associate a uno stato infiammatorio, ad oggi si conoscono anche i marcatori dell’infiammazione che si associano allo sviluppo di sarcopenia; tra questi, Interleuchina 1-beta (IL1-β), Interleuchina 6 (IL-6) e Tumor Necrosis Factor-alfa (TNF-α).
Un focus importante va sicuramente dedicato ai fattori concernenti lo stile di vita. L’aumentata sedentarietà e l’accumulo di tessuto adiposo, con conseguente obesità, sono fattori che giocano un ruolo estremamente importante nello sviluppo di sarcopenia. L’accumulo e l’eccesso di massa grassa caratteristico della condizione di obesità, infatti, determina un danno a livello del muscolo, con progressiva perdita di massa e funzione muscolare che prende il nome di obesità sarcopenica. I meccanismi fisiopatologici di questa entità rappresentano un circolo vizioso: più si accumula tessuto adiposo, più si instaurano condizioni di insulino-resistenza e di infiammazione cronica, che da un lato danneggiano il muscolo e dall’altro portano all’ulteriore accumulo di tessuto adiposo sostitutivo delle fibrocellule muscolari danneggiate.
Questo favorisce lo sviluppo di altre patologie croniche (es. diabete mellito, dislipidemie, malattie osteo-articolari, malattie cardio-vascolari), che possono impattare non solo sulla salute del muscolo, ma anche sullo stile di vita del soggetto, favorendo la sedentarietà e alimentando così un circolo vizioso. L’obesità sarcopenica è una condizione da non sottovalutare; la sua prevalenza nella popolazione anziana è di circa l’11%, anche se – come evidenziato per la sarcopenia – questa stima potrebbe variare molto in base ai metodi utilizzati per misurare la massa muscolare e la massa grassa.
Classificazione della sarcopenia
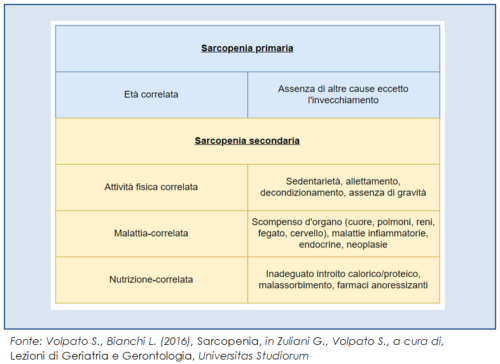
Una prima classificazione su base fisiopatologica della sarcopenia prevede la distinzione in:
- sarcopenia primaria (o “età correlata”), quando non sono riconoscibili altre cause oltre al processo di invecchiamento;
- sarcopenia secondaria, quando sono riconoscibili altre cause che possono aver determinato lo sviluppo di sarcopenia; ad esempio malattie croniche caratterizzate da stati infiammatori (neoplasie, insufficienza d’organo, malattie reumatologiche, malattie gastro-intestinali, ecc.), inattività fisica, stati di malnutrizione contraddistinti da uno scarso introito calorico e proteico.
I principali meccanismi fisiopatologici con cui si sviluppa la sarcopenia primaria sono cambiamenti ormonali, processi pro-apoptotici, meccanismi di senescenza cellulare e disfunzione mitocondriale; nella sarcopenia secondaria, invece, agisce principalmente un’infiammazione cronica.
La prevalenza di sarcopenia secondaria aumenta con l’avanzare dell’età, così come con l’età aumentano patologie e condizioni croniche (multimorbilità). Man mano che si accumulano patologie croniche nell’individuo, la maggior parte caratterizzate da uno stato di infiammazione cronica di basso grado, si osserva un aumento marcato della prevalenza di sarcopenia secondaria, soprattutto dopo i 60 anni. Le condizioni croniche maggiormente associate con la probabilità di sviluppare sarcopenia sono:
- patologie del compartimento muscolo-scheletrico;
- traumatismi;
- patologie endocrine (incluso il diabete);
- patologie neuropsichiatriche.
Un secondo tipo di classificazione della sarcopenia si basa sulla sua durata. A tale proposito distinguiamo:
- sarcopenia acuta: di durata inferiore ai 6 mesi, è generalmente una sarcopenia secondaria dovuta a condizioni acute o traumatismi che possono portare transitoriamente a una riduzione di forza e di quantità/qualità della massa muscolare; esempio tipico è dopo caduta con frattura di femore: la persona necessita di un ricovero e di un intervento chirurgico che limitano il suo livello di attività fisica, giungendo alla fine dell’iter terapeutico a un auspicabile recupero della performance fisica pre-morbosa, mediante un adeguato percorso riabilitativo;
- sarcopenia cronica: di durata superiore ai 6 mesi, è di gran lunga la tipologia più frequente; la sarcopenia cronica è generalmente un tipo di sarcopenia secondaria a condizioni progressive o legata al processo di invecchiamento.
Quest’ultima distinzione tempo-dipendente di sarcopenia sottolinea come il paziente con sarcopenia debba essere sottoposto a un’attenta rivalutazione nel tempo, per definire se si tratta di una condizione progressiva, perdurante, con uno sviluppo che si cercherà di arrestare, oppure di una condizione transitoria.
L’impatto sulla salute e sull’autosufficienza
Per processo di disabilità (disablement process) si intende quella catena di eventi fisiopatologici che portano allo sviluppo di disabilità nel soggetto anziano. Dati di letteratura suggeriscono che lo schema classico della disabilità inizi a livello di una condizione patologica che colpisce gli elementi fondamentali di un organo (cellule e tessuti). Per il paziente questo si estrinseca in un danno a livello dell’organo o dell’apparato (impairment) che si riverbera in una limitazione funzionale e in una incapacità di svolgere un’azione complessa: quando la limitazione funzionale si scontra con richieste ambientali che non possono essere soddisfatte si delinea la disabilità.
Traslando questo schema alla sarcopenia, la riduzione quantitativa e qualitativa delle fibre muscolari determina un calo della forza e ancor di più della potenza muscolare. Nel paziente si registra una limitazione funzionale, una riduzione della velocità del cammino, una ridotta capacità di salire le scale o di alzarsi da una sedia, alterazioni dell’equilibrio e, in senso generale, una riduzione globale dell’attività fisica. Nel tempo il persistere di questa condizione determina perdita delle autonomie di base e strumentali del vivere quotidiano, un aumentato rischio di cadute e, in ultima istanza, una maggiore necessità di assistenza con eventuale ricorso all’istituzionalizzazione.
Numerose evidenze scientifiche sostengono il ruolo della sarcopenia come fattore di rischio per il deterioramento dello stato funzionale generale della persona anziana. Ad esempio, uno studio di follow-up di popolazione, condotto in Toscana, ha mostrato che il rischio di sviluppare disabilità per i soggetti con sarcopenia era maggiore di circa tre volte (Bianchi, et al., 2016). Questi risultati sono stati poi riconfermati dallo stesso gruppo di ricerca in uno studio multicentrico, che ha coinvolto pazienti ricoverati in 11 centri clinici distribuiti su tutto il territorio nazionale. Tale associazione è risultata indipendente da numerosi fattori di confondimento (età, sesso, patologie croniche, ecc.) con una probabilità maggiore del 30% per i pazienti sarcopenici di essere colpiti da grave disabilità, confermando una relazione molto forte tra presenza di sarcopenia e impairment funzionale (Bianchi, et al., 2017).
Un altro aspetto fondamentale della relazione tra sarcopenia e peggioramento della funzione motoria è quello della correlazione tra sarcopenia e rischio di caduta e, soprattutto, di frattura in soggetti anziani. I soggetti con sarcopenia hanno una probabilità triplicata di andare incontro a caduta con secondarie fratture rispetto ai soggetti senza sarcopenia. Infatti, da un lato la debolezza muscolare può incidere sull’equilibrio del paziente; dall’altro le modificazioni metaboliche tipiche della sarcopenia possono influire sulla composizione dell’osso, andando a generare quella sindrome che oggi viene definita osteo-sarcopenia. La riduzione della forza muscolare e della massa muscolare, inoltre, rappresenta anche un importante fattore prognostico negativo nella possibilità di recupero riabilitativo per il soggetto anziano.
Sempre più evidenze concordano per una coesistenza tra sarcopenia e deterioramento cognitivo. I soggetti con sarcopenia hanno una probabilità quasi tre volte maggiore di presentare deterioramento cognitivo, rispetto ai soggetti che non presentano sarcopenia. Il dato estremamente interessante che emerge dagli studi porta a supporre una relazione inversa tra forza muscolare e probabilità di sviluppare malattia di Alzheimer incidente, mentre non sembra esserci alcuna relazione con la quantità di massa muscolare. Uno studio prospettico di coorte, che ha coinvolto quasi 500.000 partecipanti alla UK Biobank (età media 57 anni, oltre la metà donne) ha approfondito questo aspetto. Ne è emersa una relazione inversa e sostanzialmente lineare tra forza muscolare e rischio di sviluppare demenza, con un aumento di probabilità di sviluppare demenza del 14% per ogni 5 Kg in meno di forza muscolare (Esteban-Cornejo, et al., 2022).
Nelle ricerche degli ultimi anni è stato evidenziato un ulteriore elemento caratterizzante questa relazione: sembra infatti esserci una relazione diretta tra gravità della sarcopenia e declino cognitivo. Ulteriori studi dovranno essere effettuati per indagare questo aspetto, in quanto ad oggi i meccanismi biologici sottostanti tale associazione sono ancora oggetto di indagine, e una risposta univoca non è ancora stata identificata. Un’ipotesi è rappresentata dal fatto che il muscolo è considerato un vero e proprio organo endocrino, che produce sostanze chiamate miochine. Alcune di queste sostanze – in particolare le irsine, il Brain Derived Neurotrophic Factor (BDNF) e le catepsine – hanno un ruolo importante nella regolazione della funzione degli astrociti e della microglia cerebrale, poiché possono oltrepassare la barriera emato-encefalica.
Una delle ipotesi più forti a sostegno di una relazione causale tra sarcopenia e deterioramento cognitivo è che in presenza della patologia vi sia una riduzione di queste miochine, specie del BDNF. Tale riduzione sistemica si tradurrebbe in una riduzione di miochine a livello cerebrale, attivando l’astrocita e le cellule della microglia con sintesi e liberazione di citochine pro-infiammatorie che sarebbero responsabili del danno neuronale e, quindi, della riduzione della performance cognitiva.
La sarcopenia dunque si associa in maniera importante e significativa alle principali sindromi geriatriche: la disabilità, le cadute, le fratture, il deterioramento cognitivo. Essendo una condizione clinica così prevalente e così impattante sullo stato di salute del paziente anziano, negli ultimi anni molti ricercatori hanno voluto verificare se la sarcopenia fosse in grado anche di modulare la storia naturale di altre patologie estremamente prevalenti in ambito geriatrico, quali lo scompenso cardiaco, le cardiopatie ischemiche e la neoplasia colon-rettale.
Diversi studi hanno confermato come la sarcopenia abbia un effetto indipendente e modulatore nella traiettoria della storia naturale di varie malattie, impattando in maniera significativa sulla prognosi tanto quanto sulla sopravvivenza del paziente. Il paziente con sarcopenia è un soggetto esposto al rischio di sviluppare una serie di eventi avversi che possono portare a un aumento del rischio di mortalità: per tale motivo il paziente che presenta sarcopenia deve essere considerato un soggetto più vulnerabile e fragile.
La fragilità è una condizione dovuta a un processo di invecchiamento accelerato e alla sua interazione con le patologie del soggetto. L’interazione tra modificazioni fisiopatologiche età-correlate e patologie croniche determina una riduzione della riserva funzionale e – in situazioni particolari di stress o di aumentata richiesta funzionale all’organismo – lo sviluppo di outcome avversi come il declino funzionale, le cadute, il declino cognitivo, la disabilità, l’istituzionalizzazione e infine il decesso. Come per la sarcopenia, anche per la fragilità sono stati sviluppati e validati in letteratura numerosi strumenti per elaborare una definizione operativa e per diagnosticare la fragilità al letto del malato.
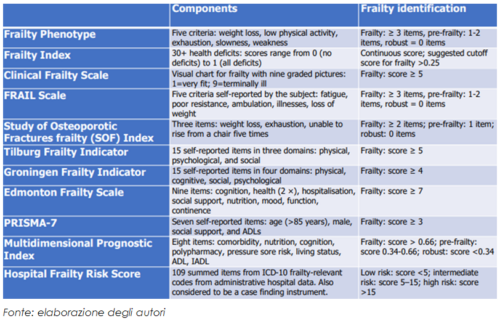
Lo strumento più utilizzato è il Frailty Phenotype (Fried, et al., 2001), che consiste di 5 criteri:
- riduzione dell’attività fisica;
- riduzione di peso involontaria;
- riduzione della forza muscolare (Grip Strength);
- riduzione del livello di energia che il soggetto è in grado di produrre;
- riduzione della velocità del cammino.
Quando sono presenti tre o più criteri la diagnosi è di fragilità; quando ve ne sono due si parla di pre-fragilità. Sarcopenia e fragilità, oltre a condividere gli stessi end-point clinici, condividono le stesse basi eziopatogenetiche, dove la stessa sarcopenia assume un ruolo fondamentale nella patogenesi della fragilità. In conclusione, nel soggetto anziano la presenza di sarcopenia predispone alla fragilità e insieme ad essa contribuisce allo sviluppo di disabilità, in un cosiddetto “ciclo della fragilità” che si autoalimenta, portando a un aumento del rischio di outcome avversi e di morte.
Bibliografia
Bianchi L., Abete P., Bellelli G., Bo M., Cherubini A., Corica F., Di Bari M., Maggio M., Manca G.M., Rizzo M.R., Rossi P.A., Landi F., Volpato S., GLISTEN Group Investigators (2017), Prevalence and clinical correlates of sarcopenia, identified according to the EWGSOP definition and diagnostic algorithm, in hospitalized older people: the GLISTEN study, in The journals of gerontology. Series A, Biological sciences and medical sciences, 12;72(11):1575-1581.
Bianchi L., Ferrucci L., Cherubini A., Maggio M., Bandinelli S., Savino E., Brombo G., Zuliani G., Guralnik J.M., Landi F., Volpato S. (2016), The predictive value of the EWGSOP definition of sarcopenia: results from the InCHIANTI study, in The journals of gerontology. Series A, Biological sciences and medical sciences, 71(2):259-264.
Clark B.C., Manini T.M. (2008), Sarcopenia =/= dynapenia, in The journals of gerontology. Series A, Biological sciences and medical sciences, 63(8):829-834.
Cruz-Jentoft A.J., Baeyens J.P., Bauer J.M., Boirie Y., Cederholm T., Landi F., Martin C.F., Michel J.-P., Rolland Y., Schneider S.M., Topinkova E., Vandewoude M., Zamboni M. (2010), Sarcopenia: European consensus on definition and diagnosis. Report of the European Working Group on Sarcopenia in Older People, in Age and Ageing, 39(4):412-423.
Cruz-Jentoft A.J., Bahat G., Bauer J., Boirie Y., Bruyère O., Cederholm T., Cooper C., Landi F., Rolland Y., Sayer A.A., Schneider S.M., Sieber C.C., Topinkova E., Vandewoude M., Visser M., Zamboni M. (2019), Sarcopenia: revised European consensus on definition and diagnosis, in Age and Ageing, 1;48(1):16-31.
Esteban-Cornejo I., Frederick K.H., Petermann-Rocha F., Lyall D.M., Martinez-Gomez D., Cabanas-Sánchez V., Ortega B.F., Hillman C.H., Gill J.M.R., Quinn T.J., Sattar N., Pell J.P., Gray S.R., Celis-Morales C. (2022), Handgrip strength and all-cause dementia incidence and mortality: findings from the UK Biobank prospective cohort study, in Journal of Cachexia, Sarcopenia and Muscle, 13(3):1514-1525.
Fried L.P., Tangen C.M., Walston J., Newman A.B., Hirsch C., Gottdiener J., Seeman T., Tracy R., Kop W.J., Burke G., McBurnie M.A., Cardiovascular Health Study Collaborative Research Group (2001), Frailty in older adults: evidence for a phenotype, in The journals of gerontology. Series A, Biological sciences and medical sciences, 56(3):M146-156.
Rosenberg I.H. (1997), Sarcopenia: origins and clinical relevance, in The Journal of Nutrition,127(5 Suppl):990S-991S.
Studenski S.A, Peters K.W., Alley D.E., Cawthon P.M., McLean R.R., Harris T.B., Ferrucci L., Guralnik J.M., Fragala M.S., Kenny A.M., Kiel D.P., Kritchevsky S.B., Shardell M.D., Dam T.-T.L., Vassileva M.T. (2014), The FNIH sarcopenia project: rationale, study description, conference recommendations and final estimates, in The journals of gerontology. Series A, Biological sciences and medical sciences, 69(5):547-558.
Trevisan C., Vetrano D.L., Calvani R., Picca A., Welmer A.-K. (2022), Twelve-year sarcopenia trajectories in older adults: results from a population-based study, in Journal of Cachexia, Sarcopenia and Muscle, 13(1):254-263.












